Berlin, 12. Juni 2012: Die Forschung der letzten Jahre hat gezeigt, dass ein breites Spektrum an Zytokinen und Immunzellen an der Pathogenese der Rheumatoiden Arthritis beteiligt ist. Die Ergebnisse unterstreichen die Bedeutung von Zytokin-Netzwerken und zentralen Umschaltstellen in den intrazellulären Signalwegen. Die derzeit in der Entwicklung befindlichen neuen Wirkstoffe sind „small molecules“, die gezielt die intrazelluläre Signalvermittlung von wichtigen pro-inflammatorischen Zytokinen hemmen. Bisherige Therapieansätze wie Biologika zielen auf einzelne Moleküle wie z.B. Tumornekrosefaktor alpha (TNF-) und hemmen die Wirkung von Zytokinen im extrazellulären Raum. Einer der zentralen intrazellulären Signalwege sind die der Janus-Kinasen (JAKs).
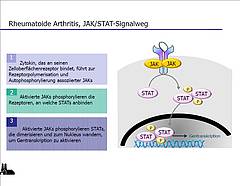
Abb.1 Der JAK/STAT-Signalweg. Vortrag Prof. H. Schulze-Koops, Leiter der Rheumaeinheit, Klinikum der Ludwig- Maximilians-Universität München. Pfizer-Pressegespräch „Intrazelluläre Targets in der Rheumatoiden Arthritis: Die intrazellulären Signalwege der Janus-Kinasen“ am 7. Juni 2012 in Berlin.

Abb. 2 Das ORAL-Studienprogramm. Vortrag Dr. Rieke Alten, Chefärztin der Abteilung für Rheumatologie, Schlosspark-Klinik Berlin. Pfizer-Pressegespräch „Intrazelluläre Targets in der Rheumatoiden Arthritis: Die intrazellulären Signalwege der Janus-Kinasen“ am 7. Juni 2012 in Berlin.
Tofacitinib (CP-690,550) ist ein oraler JAK-Inhibitor, der derzeit in einem umfangreichen klinischen Studienprogramm als zielgerichteter Immunmodulator für die krankheitsmodifizierende Therapie der Rheumatoiden Arthritis untersucht wird. Im Rahmen eines Pressegesprächs von Pfizer stellten Experten den neuen Wirkansatz und aktuelle Daten aus dem Studienprogramm vor.
Der Schwerpunkt der wissenschaftlichen Forschung in der Rheumatologie lag in den letzten Jahren auf den intrazellulären Signalwegen der Zytokine. Seitdem die zentrale Rolle von Zytokinen für die Pathogenese von chronisch entzündlichen Erkrankungen wie der Rheumatoiden Arthritis (RA) belegt ist, sind sie zu Targets einer gezielten krankheitsmodifizierenden Therapie geworden.1, 2
Biologika waren ein wichtiger Schritt in diese Richtung. Sie können die überschießende Immun- und Entzündungsreaktion effektiv inhibieren, indem sie gezielt ein Zytokin, wie zum Beispiel TNF-, im Extrazellularraum inhibieren. Die nun in der klinischen Entwicklung befindlichen „small molecules“ greifen dagegen intrazellulär in die Weiterleitung von Zytokinsignalen unterschiedlicher an der Pathogenese der RA beteiligter Zytokine ein. Sie blockieren die Weiterleitung des Signals von der Zelloberfläche in den Zellkern von Immunzellen.3
„Einer dieser Signaltransduktionswege, der von einer wichtigen Untergruppe proinflammatorischer Zykotine benutzt wird, ist der Signalweg der Janus-Kinasen (JAKs)“, erläuterte Prof. Hendrik Schulze-Koops, München. „Er scheint als Drehscheibe für diverse Zytokin-vermittelte Signale zu fungieren und hat sich als wichtig für die Entwicklung, das Überleben, die Proliferation und Differenzierung von Immunzellen sowie die Vermittlung der entzündlichen Immunantwort gezeigt“, so Schulze-Koops weiter.2
Hemmung intrazellulärer Signalkaskaden von pro-inflammatorischen Zytokinen
Sobald Zytokine an ihre spezifischen Rezeptoren binden, werden die Janus-Kinasen, von denen es vier gibt, die jeweils paarweise zusammenarbeiten (JAK 1, JAK 2, JAK 3 und Tyrosin-Kinase 2 (TYK 2)), aktiviert. Es kommt zunächst zur Autophosphorylierung mit anschließender Aktivierung (Phosphorylierung) eines weiteren intrazellulären Proteins, das als Signaltransduktor und Aktivator der Transkription (STAT) bezeichnet wird. STATs dimerisieren daraufhin und wandern in den Zellkern (Translokation). Dort fördern sie die Transkription von Genen auch pro-inflammatorischer Zytokine und Chemokine, die wiederum die Produktion, Differenzierung, Aktivität und Rekrutierung von Immunzellen in die Synovia fördern (Abb.1).
„Daher stellt die Inhibition des Janus-Kinase-Signalwegs eine Rationale in der Therapie von chronisch-entzündlichen Erkrankungen dar. Im Vergleich zu extrazellulären Inhibitoren eines einzelnen spezifischen Zytokins können mit JAK-Inhibitoren die Signale diverser Zytokine, darunter der Interferone IFN IFN sowie der Interleukine IL-6, IL-7, IL-10, IL-12, IL-15, IL-17 und IL-23, moduliert werden“, erklärte Schulze-Koops den Zusammenhang. Voraussichtlich lässt sich so ein Effekt auf die vielfältigen Aspekte der RA-typischen Immunreaktion erzielen.
Tofacitinib, ein JAK-Inhibitor in der klinischen Prüfung
Tofacitinib (CP-690,550) ist der bisher in der klinischen Prüfung am weitesten fortgeschrittene JAK-Inhibitor und inhibiert in vitro JAK 1, JAK 2 und JAK 3 sowie in geringerem Ausmaß TYK2, wobei er eine funktionelle Spezifität für JAK 1 und JAK 3 gegenüber JAK 2 aufweist.
Der JAK-Inhibitor Tofacitinib kann oral eingenommen werden und wird derzeit in einem großen Phase III-Studienprogramm (ORAL, Oral Rheumatoid Arthritis phase 3 triaLs) untersucht (Abb. 2).
Dr. Rieke Alten, Berlin, ging näher auf das ORAL-Studienprogramm ein: „Weltweit wurden bisher etwa 4.000 erwachsene Patienten mit mittelschwerer bzw. schwerer aktiver Rheumatoider Arthritis behandelt, und am Kernprogramm sind 350 Studienzentren in 45 Ländern beteiligt.“ Das Phase III-Studienprogramm zum JAK-Inhibitor Tofacitinib umfasst fünf abgeschlossene Studien und eine noch laufende Studie. „Zudem wird die Wirksamkeit und Sicherheit von Tofacitinib in zwei offenen Langzeit-Extensionsstudien untersucht“, ergänzte Alten.
Alle sechs Phase III-Studien des ORAL-Studienprogramms haben ein ähnliches Studiendesign: Es sind randomisierte, doppelblinde, placebokontrollierte Studien, in denen die Studienteilnehmer den Janus-Kinase-Inhibitor Tofacitinib in der Dosierung von zweimal täglich 5 bzw. 10 mg erhielten. Patienten der Placebogruppe wurden je nach Laufzeit der Studie entweder nach drei oder sechs Monaten randomisiert und weiter verblindet auf zweimal täglich 5 mg oder 10 mg Tofacitinib umgestellt. Tofacitinib wurde sowohl als Monotherapie, als auch in Kombination mit DMARDs (Disease Modifying Anti-Rheumatic Drugs) bzw. Methotrexat (MTX) geprüft. Die Dauer der Studien betrug sechs, zwölf bzw. 24 Monate.3
Als primäre Studienendpunkte wurden bei allen Studien das ACR20-Ansprechen, die mittlere Veränderung der körperlichen Funktionsfähigkeit gemessen anhand des HAQ-DI sowie das Erreichen einer Krankheitsaktivität von <2,6 auf Basis eines DAS28-4 gewählt. In zwei Studien mit kam mit dem mTSS (modified Total Sharp Score) ein radiologischer primärer Endpunkt hinzu.
Aktuell präsentierte Daten zum Studienprogramm auf dem EULAR
Anlässlich des Kongresses der European League Against Rheumatism (EULAR) in Berlin wurden weitere Daten aus dem Phase III-Studienprogramm vorgestellt:
• In der Subgruppenanalyse von 3.442 Patienten aus den gepoolten Daten der
Phase II- und III-Studien zu verschiedenen Wirksamkeitsendpunkten 6
erwies sich Tofacitinib unabhängig von den demographischen und
krankheitsspezifischen Charakteristika der RA-Patienten als wirksam. Alter,
Geschlecht, Körpergewicht, Body-Mass-Index, Ethnie, geographische Region,
Dauer der Erkrankung, serologischer Status, Krankheitsaktivität und
vorangegangene Therapieregime waren ohne Einfluss auf das ACR20-
Ansprechen, also eine mindestens 20%ige Verbesserung der
Krankheitszeichen und Symptome gegenüber dem Ausgangswert, gemessen
mit der Skala des American College of Rheumatology (ACR), und die mittlere
Veränderung der körperlichen Funktionsfähigkeit, gemessen mit dem HAQ-DI
(Health Assessment Questionnaire-DIsablity Index).
• Die Auswertung zu den Patient Reported Outcomes (PROs)7 aus einer Studie
des ORAL-Studienprogramms (ORAL Standard), in der die Wirksamkeit von
Tofacitinib (2 x 5 bzw. 2 x 10 mg/d) nicht nur mit der von Placebo, sondern
auch von Adalimumab verglichen wurde, zeigte nach sechs Monaten eine im
Vergleich zu Placebo statistisch signifikante Verbesserung aller PROs unter
Tofacitinib und Adalimumab. Untersucht wurden PROs zu den Domänen
Fatigue (FACIT-F) und Schlaf (MOS Sleep Scale), Gesamtbeurteilung der
Krankheitsaktivität durch den Patienten (PtGA [VAS]), Schmerz (pain-VAS),
körperliche Funktion (HAQ-DI) und Lebensqualität (HR-QoL). In dieser
randomisierten Phase III-Studie waren RAPatienten eingeschlossen, die nicht
auf MTX ansprechen. Die PROs wurden Rahmen der ORAL Standard-Studie als
sekundäre Endpunkte gemessen.
Quelle: Pfizer-Pressegespräch „Intrazelluläre Targets in der Rheumatoiden Arthritis: Die intrazellulären Signalwege der Janus-Kinasen“ am 7. Juni 2012 in Berlin
Literatur
1. McInnes IB, Schett G: Cytokines in the pathogenesis of rheumatoid arthritis.
Nat Rev Immunol 2007;7(6):429-442. Abstract
2. Leonard WJ: Cytokines and immunodeficiency diseases. Nat Rev Immunol
2001;1(3):200-208. Full Text
3. Mavers M, Ruderman EM, Perlman H: Intracellular signal pathways: potential
for therapies. Curr Rheumatol Rep 2009;11(5):378-385. Abstract
4. Ghoreschi K, Laurence A, O’Shea JJ: Janus kinases in immune cell signaling.
Immunol Rev 2009;228(1):273-287. Full Text
5. Riese RJ, Krishnaswami S, Kremer J: Inhibition of JAK kinases in patients with
rheumatoid arthritis: scientific rationale and clinical outcomes. Abstract
Best Pract Res Clin Rheumatol 2010;24(4):513-526.
6. Kremer J et al.: Tofacitinib (CP-690,550), an oral Janus Kinase Inhibitor:
Analysis of efficacy endpoints by subgroups in a pooled phase 2 and 3
rheumatoide arthrtisstudy population. EULAR 2012: Poster THU0143
7. van Vollenhoven RF et al.: Effects of Tofacitinib (CP-690,550), an oral Janus
Kinase Inhibitor, or Adalimumab on patient reported outcomes in a phase 3
study of active rheumatoid arthritis. EULAR 2012: THU0151
