RAPID-1 (Rheumatoid Arthritis: PreventIon of structural Damage) ist eine 52-wöchige, zulassungsrelevante, randomisierte, doppelblinde, placebo-kontrollierte internationale multizentrische Phase-III-Studie zur Prüfung der Wirksamkeit und Verträglichkeit von zwei unterschiedlichen Dosierungen (200 mg und 400 mg alle 2 Wochen s.c.) von Certolizumab Pegol (Cimzia) in Kombination mit Methotrexat (MTX) im Vergleich zu einer MTX-Monotherapie bei Patienten mit einer rheumatoiden Arthritis (RA) nach vorhergehendem MTX-Versagen. Im Unterschied zu RAPID-2 wurde dabei Certolizumab Pegol nicht in flüssiger Form als Fertigspritze, sondern als Lyophilisat (Trockenpulver mit Lösung zum Zusammenmischen) angewendet.
Studienziele waren die Verbesserung der klinischen Symptome einer aktiven RA, die Verbesserung der Funktionskapazität und der Lebensqualität sowie eine Hemmung der Röntgenprogression, d.h. das Aufhalten von entzündlich bedingten Gelenkschäden.
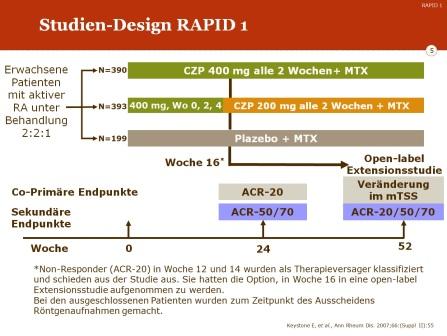
Als primäre Endpunkte wurden die ACR-20-Responder-Rate in Woche 24 und die radiologische Progression in Woche 52 definiert (gemessen über den modifizierten Total Sharp Score, mTSS).
Sekundäre Endpunkte waren
- die radiologische Progression in Woche 24 definiert (gemessen über den modifizierten Total Sharp Score, mTSS)
- die ACR-20-Responder-Rate in Woche 52
- die ACR-50- und ACR-70-Responder-Raten in Woche 24 und Woche 52
- das DAS-28-Ansprechen in Woche 24 und Woche 52
- die Verbesserung der Funktionskapazität in Woche 24 und Woche 52 (gemessen im HAQ-DI) und
- die Verbesserung der Lebensqualität in Woche 24 und Woche 52 (gemessen im SF-36).
Aufgenommen in die Studie wurden 982 erwachsene RA-Patienten im Alter von ≥ 18 Jahren (Klassifikation der RA nach den ACR-Kriterien von 1987)) mit einer Krankheitsdauer von ≥ 6 Monaten und < 15 Jahren. Alle Patienten mussten eine aktive Erkrankung aufweisen, d.h. mindestens 9 druckschmerzhafte Gelenke, mindestens 9 geschwollene Gelenke, eine BSG (nach Westergren) von ≥ 30 mm/h oder ein CRP von > 15 mg/l.
Die Patienten hatten zuvor auf eine ausreichend lange durchgeführte und ausreichend hoch dosierte Therapie mit Methotrexat (MTX) nicht oder nicht ausreichend angesprochen („MTX-Versager“), wobei ein MTX-Versagen über eine fehlende oder unzureichende Wirkung von MTX unter einer Dosis von mindestens 10 mg MTX pro Woche und nach einer Therapiedauer von mindestens 6 Monaten definiert war.
Zu Studienbeginn mußte MTX für mindestens 2 Monate in einer stabilen Dosis verabreicht worden sein.
Eine Therapie mit Cortison war erlaubt, wobei ein Prednison-Äquivalent von ≤ 10 mg/Tag nicht überschritten werden durfte.
Ein Ausschlußgrund für die Aufnahme in die Studie war eine unmittelbar vorausgegangene Therapie mit einem anderen TNF-alpha-Blocker bzw. einem anderen Biologikum (im Zeitraum von 6 Monaten vorher; bei Etanercept und Anakinra 3 Monate vorher) sowie ein TNF-Versagen in der Anamnese.
Die Patienten wurden in einem Verhältnis von 2:2:1 auf die drei Studienarme aufgeteilt („randomisiert“):
- 390 Patienten erhielten Certolizumab Pegol (CPZ) in einer Dosis von 400 mg alle 2 Wochen in Kombination mit MTX (Fortführung der vorbestehenden wöchentlichen stabilen MTX-Dosis)
- 393 Patienten erhielten Certolizumab Pegol (CPZ) in einer Dosis von 200 mg alle 2 Wochen in Kombination mit MTX (Fortführung der vorbestehenden wöchentlichen stabilen MTX-Dosis)
- 199 Patienten erhielten alle 2 Wochen Placebo in Kombination mit MTX (Fortführung der vorbestehenden wöchentlichen stabilen MTX-Dosis)
Patienten, die nach 12 und 14 Wochen kein ACR-20-Ansprechen erreicht hatten, wurden als Therapieversager klassifiziert und schieden aus dem ursprünglichen Behandlungsprotokoll aus. Sie hatten allerdings die Möglichkeit, in eine offene Studie (open-label-Extensions-Studie) aufgenommen zu werden und bekamen dann ab der 16. Woche 400 mg Certolizumab Pegol alle 14 Tage in Kombination mit wöchentlich verabreichtem MTX. Um eine Aussage zur radiologischen Progression zu bekommen, wurden bei ihnen zu diesem Zeitpunkt Röntgenaufnahmen von Händen und Füßen durchgeführt.
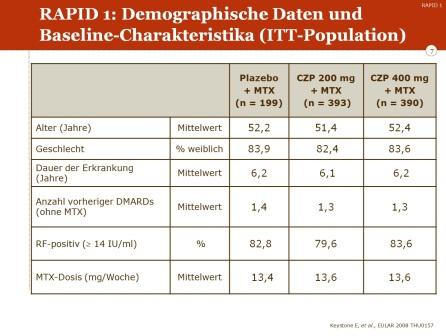
Zu Studienbeginn wiesen die Patienten mit durchschnittlich etwa 52 Jahren das typische Alter auf, das man in vergleichbaren Studienpopulationen sieht. Im Mittel lag die Krankheitsdauer bei ca. 6 Jahren, d.h. die Erkrankung war zu diesem Zeitpunkt bereits fortgeschritten. Neben MTX waren die Patienten vor Einschluß in die Studie in der Regel mit einem weiteren DMARD vorbehandelt worden. Mehr als ¾ der Patienten waren seropositiv (Rheumafaktor-positiv). Die mittlere MTX-Dosis betrug 13,5 mg pro Woche.
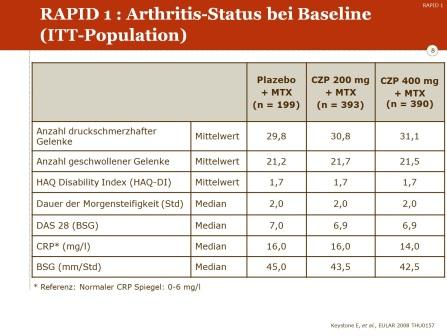
Die Erkrankung war vor Beginn der Studie mit durchschnittlich 30 druckschmerzhaften und mehr als 20 geschwollenen Gelenken hochaktiv; dies spiegelt sich auch in einem hohen DAS-28 von fast 7 Einheiten und in einer hohen systemischen Entzündungsaktivität wieder (BSG über 40 mm/h n.W.).
Mit einem HAQ-DI von 1.7 war die Funktionskapazität bereits erheblich eingeschränkt.
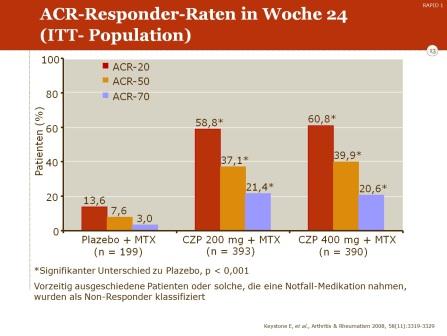
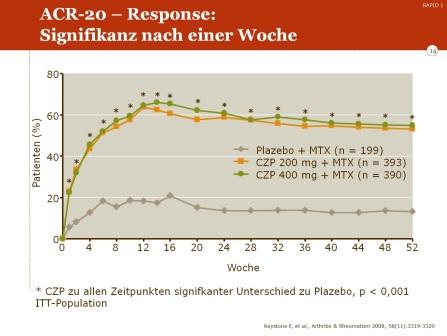
Nach einem Behandlungszeitraum von 24 Wochen erreichten 58,8% der Patienten unter 200 mg Certolizumab Pegol plus MTX und 60,8% unter 400 mg Certolizumab Pegol plus MTX ein ACR-20-Ansprechen gegenüber nur 13,6% der Patienten in der Placebo-Gruppe. Nur eine geringe Zahl der Patienten in der Placebo-Gruppe erreichten ein ACR-50- und ACR-70-Ansprechen; unter der Certolizumab-MTX-Kombination betrugen diese Raten 37,1%/39,9% für ACR-50 (bei 200 mg bzw. 400 mg Certolizumab) sowie 21,4%/20,6% für die ACR-70-Response.
Die Wirkung der Certolizumab-MTX-Kombination trat sehr schnell ein. Ein signifikanter Unterschied im ACR-20-Ansprechen zeigte sich bereits nach einer Woche. Ebenso war bereits nach einer Woche ein signifikanter Rückgang bei der Zahl geschwollener und bei der Zahl schmerzhafter Gelenke zu beobachten.
Eine signifikante Verbesserung im Vergleich zu Placebo war auch weitere klinische Parameter zu verzeichnen: Reduktion der Schmerzen, Abnahme von Müdigkeit und Erschöpfung („fatigue“) sowie insgesamt eine Zunahme der Lebensqualität.
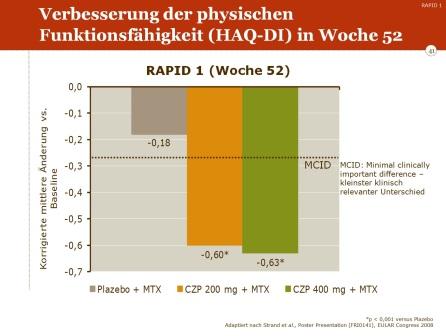
Parallel zum klinischen Ansprechen sieht man unter der Certolizumab-MTX-Kombination eine deutliche Besserung der funktionellen Kapazität, d.h. eine Abnahme der krankheitsbedingten Behinderung.
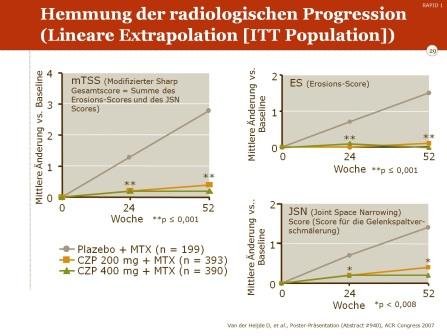
Durch die Certolizumab-MTX-Kombination konnte die radiologische Progression gegenüber Placebo signifikant gehemmt werden. Sowohl im Erosions-Score als auch im Score für die Gelenkspaltverschmälerung zeigte sich ein praktisch vollständiger Stop der radiologischen Progression. Für den Gelenkspalt-Score und den Gesamt-Score waren die Ergebnisse von Woche 24 bis Woche 52 tendenziell besser unter der höheren Certolizumab-Dosierung von 400 mg alle 14 Tage.
Erwähnenswert ist eine Diskrepanz zwischen dem klinischen Ansprechen und den radiologischen Daten.
Eine Zusatzauswertung der radiologischen Daten von denjenigen Patienten, die wegen eines fehlenden klinischen Ansprechens (ACR-20 nicht erreicht) in der 16. Woche aus der verblindeten Studie herausgenommen worden waren, zeigte unabhängig davon eine Verzögerung der Röntgenprogression unter Certolizumab Pegol. Dies ist zugleich ein Hinweis darauf, daß die Hemmung der Röntgenprogression unter Certolizumab sehr rasch einsetzt.
Die bislang für die Therapie der rheumatoiden Arthritis eingesetzten TNF-alpha-Blocker sind entweder monoklonale Antikörper (Infliximab, Adalimumab, Golimumab) oder lösliche Rezeptoren (Etanercept). Allen gemeinsam ist ein Immunglobulin-G-Fc-Anteil. Die Daten der Rapid-2-Studie zeigen, daß dieser IgG-Fc-Anteil offensichtlich keine Bedeutung für die Wirksamkeit eines TNF-alpha-Blockers hat, denn Certolizumab Pegol kommt als pegylierter Antikörper ohne einen solchen Anteil aus. Die Wirksamkeit der TNF-alpha-Blockade ist demnach offensichtlich auch durch ein Fc-freies Fab-Fragment wie durch Certolizumab Pegol möglich.
Die Verträglichkeit und Sicherheit von Certolizumab Pegol entsprach in der RAPID-1-Studie den Daten, die auch von den anderen TNF-alpha-Blockern bekannt sind.
Nennenswerte unerwünschte Wirkungen waren eine etwas erhöhte Infektionsrate einschließlich schwerwiegender Infektionen und einzelner Tuberkulosefälle. Die Infektionen betrafen zumeist die oberen Luftwege (Erkältungen, Nebenhöhlenentzündungen, Bronchitis) sowie den Urogenitaltrakt (Harnwegsinfekte).
Hinsichtlich der Verträglichkeit erwähnenswert ist die unter Certolizumab Pegol im Vergleich mit anderen, subkutan verabreichten Medikamenten sehr niedrige Rate an lokalen Reaktionen am Injektionsor
Referenzen:
Keystone E, Heijde D, Mason D Jr, Landewé R, Vollenhoven RV, Combe B, Emery P, Strand V, Mease P, Desai C, Pavelka K.
Certolizumab Pegol plus methotrexate is significantly more effective than placebo plus methotrexate in active rheumatoid arthritis: findings of a fifty-two-week, phase III, multicenter, randomized, double-blind, placebo-controlled, parallel-group study.
Arthritis Rheum. 2008 Nov;58(11):3319-29
Abstract
Volltext