Zusammenfassung
Tocilizumab in Kombination mit DMARDs zeigte in Studien im Vergleich zu DMARDs plus Placebo eine sehr gute Wirksamkeit hinsichtlich klinischer und radiologischer Daten.
OPTION und TOWARD
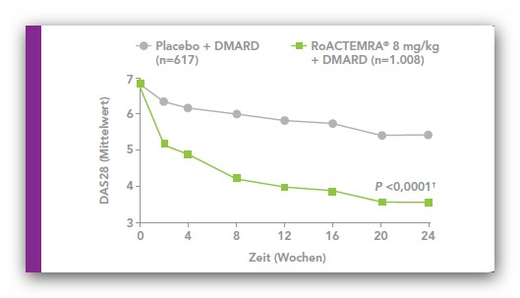
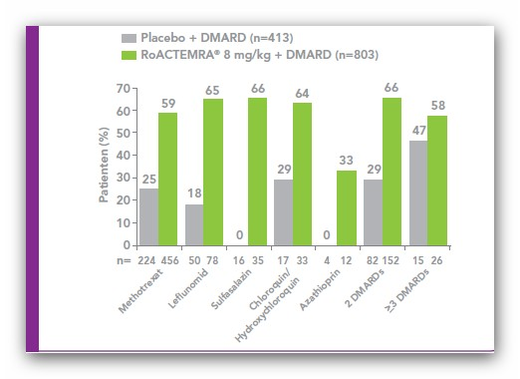
In der zulassungsrelevanten Phase III Studie OPTION wurde Tocilizumab bei Patienten mit aktiver rheumatoider Arthritis (RA) gegeben, die unzureichend auf Methotrexat (MTX) angesprochen hatten. In der ebenfalls zulassungsrelevanten Phase III Studie TOWARD galt das gleiche, nur dass in dieser Studie auch Patienten mit Therapieversagen unter weiteren DMARDs (Chloroquin, Hydroxychloroquin, parenterales Gold, Sulfasalazin, Azathioprin und Leflunomid) zugelassen waren.
In beiden Studien erhielten die Patienten entsprechend der Randomisierung über einen Zeitraum von 24 Wochen eine DMARD-Basistherapie in Kombination mit Tocilizumab oder Placebo in 4-wöchentlichen Abständen.
Die Studien unterschieden sich in den eingesetzten Dosen von Tocilizumab und der erlaubten DMARD-Therapie.
LITHE
In einer dritten Phase-III-Studie LITHE über 2 Jahre wurden 1.196 Patienten mit mäßig schwerer bis schwerer RA untersucht, die unzureichend auf Methotrexat ansprachen [3]. Zusätzlich zu einer konstanten Dosis an Methotrexat erhielten die Patienten alle 4 Wochen verblindet entweder Tocilizumab 4 mg/kg oder 8 mg/kg oder Placebo über einen Zeitraum von 52 Wochen.
Patienten der Behandlungsgruppe mit Tocilizumab 8 mg/kg wiesen im Vergleich zur Placebo-Gruppe signifikante Verbesserungen der klinischen Symptome auf und hatten entsprechend signifikant bessere ACR-Ansprechraten in Woche 24 und 52.
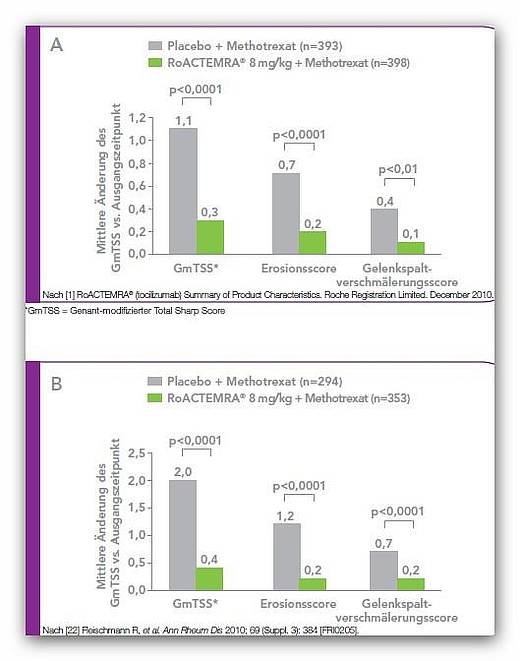
Patienten, die mit Tocilizumab 8 mg/kg behandelt wurden, zeigten über einen Zeitraum von A) 52 Wochen und B) 104 Wochen eine signifikant geringere radiologische Progression als die Patienten in der Kontrollgruppe (Abb. 3) [4].
TAMARA
In der TAMARA-Studie wurde die Wirksamkeit und Sicherheit von Tocilizumab unter den Bedingungen der täglichen Praxis überprüft. Die Studie wurde in Deutschland einarmig und multizentrisch (70 Zentren) durchgeführt [5].
Insgesamt wurden 286 Patienten mit aktiver rheumatoider Arthritis mit 8mg/kg Tocilizumab behandelt. 277 Patienten erhielten therapiebegleitend DMARDs (Methotrexat (MTX), Leflunomid, Sulfasalazin) über einen Zeitraum bis zu 24 Wochen.
Bis auf einen Patienten waren alle mit DMARDs vorbehandelt: meistens mit Methotrexat (95,1 %) oder mit Leflunomid (60,1 %). Während der Studie wurde MTX bei 72,0 % und Leflunomid bei 19,6 % der Patienten weiter gegeben.
Die ACR Responseraten zu Woche 24 zeigen, dass 65,0 Prozent der Patienten die ACR20-Kriterien erfüllten, 50,7 Prozent die ACR50-und 33,9 Prozent aller Patienten die ACR70-Kriterien erfüllten.
Bei getrennter Betrachtung der Patienten, die zuvor mit DMARDs erfolglos behandelt worden waren, sieht man auch bei diesem Kollektiv ein ebenfalls gutes Therapieansprechen ungeachtet der Vorbehandlung (Tab. 1)
| Studienbeginn | 4 Wochen | 24 Wochen | |
| Geschwollene Gelenke | 13,3±7,3 | 6,2±7,1 | 3,8±4,9 |
| Schmerzhafte Gelenke | 20,0±11,2 | 10,1±11,4 | 5,3±8,4 |
| CRP (mg/l) | 20,7±32,2 | 45±12,8 | 3,3±9,5 |
| BSG (mm/h) | 35,6±20,3 | 9,3±12,5 | 6,9±9,1 |
| Krankheitsaktivität Arzt (VAS, mm) | 61,2±19,4 | 27,9±20,2 | 13,2±14,9 |
| Krankheitsaktivität Pat. (VAS, mm) | 60,4±21,5 | 38,0±26,7 | 23,6±26,3 |
| HAQ-DI | 1,33±0,65 | 1,01±0,69 | 0,84±0,724 |
Patienten, die zuvor auf DMARDs unzureichend angesprochen hatten, reagierten mit einer besseren klinischen Therapieantwort als Patienten mit einem vorherigen unzureichendem Ansprechen auf TNF-Inhibitoren – ein Ergebnis, das zu erwarten war, da letztere Patienten länger und schwerer an der RA erkrankt waren, bevor auf Tocilizumab gewechselt wurde.
Literatur
EULAR 2008 – FRI0172 Smolen J, et al. Tocilizumab rapidly and significantly reduces DAS28 in patients with rheumatoid arthritis inadequately responding to DMARDs: Pooled analysis
Genovese MC, McKay JD, Nasonov EL, et al. Interleukin-6 receptor inhibition with tocilizumab reduces disease activity in rheumatoid arthritis with inadequate response to disease-modifying antirheumatic drugs: Tocilizumab in combination with traditional disease-modifying antirheumatic drug therapy study. Arthritis Rheum. 2008;58:2968–2980. http://www.ncbi.nlm.nih.gov/pubmed/18821691
RoACTEMRA® (tocilizumab) Summary of Product Characteristics. Roche Registration Limited. December 2010
EULAR 2009 - FRI0205 Fleischmann R, et al. Tocilizumab Inhibits Radiologic Progression, Improves Physical Function, And Gains Efficacy over Time: LITHE 2 Year
Gerd R Burmester, E Feist, H Kellner, J Braun, C Iking-Konert, A Rubbert-Roth: Effectiveness and safety of the interleukin 6-receptor antagonist tocilizumab after 4 and 24 weeks in patients with active rheumatoid arthritis: the first phase IIIb real-life study (TAMARA), Ann Rheum Dis doi:10.1136/ard.2010.139725 Published Online First 27 December 2010
Full Text