Inhalt
Studien zur Sicherheit von Anakinra (Kineret) bei der rheumatoiden Arthritis
Die Sicherheit von Anakinra (Handelsname: Kineret) bei der Therapie der rheumatoiden Arthritis (chronischen Polyarthritis) wurde in 3 randomisierten, placebo-kontrollierten Studien mit insgesamt 2.932 Patienten mit rheumatoider Arthritis sowie in einer speziellen Studie zur Langzeitanwendung in der täglichen Praxisroutine überprüft. Die Erfahrungen aus dieser Sicherheitsstudie beziehen sich auf 1.199 Patienten mit rheumatoider Arthritis. Das Nebenwirkungsprofil von Anakinra in der Kombination mit Methotrexat (MTX) gibt die nachfolgende Tabelle wieder.
Nebenwirkungsprofil von Anakinra. Prozentsätze der häufigsten Nebenwirkungen (Prozent der Patienten), die von Patienten mit rheumatoider Arthritis in der Kombinationstherapie mit Methotrexat (Mtx) angegeben wurden.
| Placebo | Anakinra 100 mg/Tag + Mtx | |
| Patientenzahl | (N = 733) | (N = 1565) |
| Injektionsreaktionen | 29% | 71% |
| Infektionen | 37% | 39% |
| - Obere Luftwege | 17% | 14% |
| - Sinusitis | 7% | 7% |
| - grippeartige Symptome | 6% | 6% |
| Gelenkschmerzen | 6% | 6% |
| Kopfschmerzen | 9% | 12% |
| Übelkeit | 7% | 8% |
| Durchfall | 5% | 7% |
| Bauchschmerzen | 5% | 5% |
(berücksichtigt sind alle Nebenwirkungen, die in einer Häufigkeit von > 5% auftraten)
Die umfangreiche, spezielle Sicherheitsstudie sammelte Daten von Patienten mit rheumatoider Arthritis, die neben Anakinra eine ganze Anzahl unterschiedlicher weiterer langwirksamer Antirheumatika im Sinne von Kombinationstherapien erhielten, daneben auch von Patienten, die mit einer Anakinra-Monotherapie behandelt wurden. Die in der Kombination eingesetzten Substanzen umfassten Methotrexat (Mtx), Sulfasalazin, Hydroxychloroquin, Gold, D-Penicillamin, Leflunomid und Azathioprin. Ausgeschlossen in dieser Studie waren allerdings Patienten, die in einer Kombination mit TNF-alpha-Blockern behandelt wurden.
Eine ganze Anzahl von Patienten in dieser Studie hatten aufgrund von Vorerkrankungen oder Begleiterkrankungen bereits eingangs ein erhöhtes Infektionsrisiko. So nahmen auch Patienten mit vorausgegangener Lungenentzündung sowie Patienten mit Diabetes mellitus (Zuckerkrankheit), Asthma oder chronisch-obstruktiven Lungenerkrankungen an der Sicherheitsstudie teil.
Rolle der Komorbidität bei Hochrisiko-Patienten mit aktiver rheumatoider Arthritis
Ziel einer weiteren, post hoc-durchgeführte Analyse war es, das Sicherheitsprofil der täglichen Behandlung mit Anakinra bei Hochrisiko-Patienten mit aktiver rheumatoider Arthritis und Begleiterkrankungen, sogenannten Komorbiditäten, zu überprüfen. Dies geschah in einer großen, randomisierten, placebo-kontrollierten und doppelt verblindeten Studie über sechs Monate. Um die klinische Praxis möglichst realitätsnah abzubilden, waren die Einschlusskriterien der Studie weit gefasst.
In jeder Behandlungsgruppe (Anakinra, n=1116 oder Placebo, n=283), wurden die Inzidenzraten für schwerwiegende unerwünschte Ereignisse (SUE), infektiöse Ereignisse, (IE) und schwer wiegende infektiöse Ereignisse (SIE) bei Hochrisiko-Patienten zusammengefasst und mit den Raten der Patienten ohne Begleiterkrankungen verglichen.
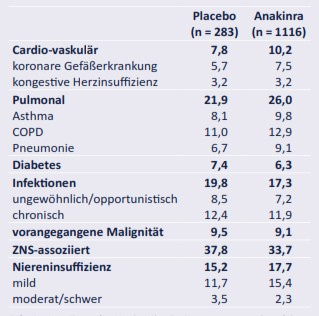
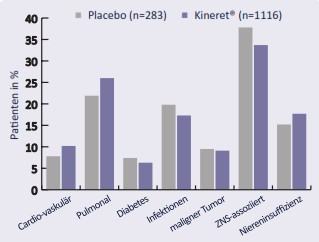
Zu den Patienten mit einem hohen Risiko für das Auftreten von unerwünschten Nebenwirkungen zählten die, bei denen in der Anamnese eine oder mehrere der in Tabelle 2 aufgeführten Erkrankungen aufgetreten waren. Die Tabelle zeigt außerdem die Verteilung der Hochrisiko-Patienten innerhalb der Untergruppen der Begleiterkrankungen.
Aufgrund von Berichten aus Studien zu anderen antirheumatischen Biologika wurde auf die Dokumentation des Auftretens von schwerwiegenden oder weniger schwerwiegenden Infektionen großen Wert gelegt.
Bei Studienbeginn waren die Studiengruppen in punkto Begleitmedikation, Dauer der rheumatoiden Arthritis, Geschlecht und Alter sowie der Anzahl empfindlicher/schmerzhafter/geschwollener Gelenke ausgeglichen. Der größte Teil der Patienten (insgesamt 68%; 69,3% Placebo und 67,7% Anakinra) wies eine oder mehrere Begleiterkrankungen auf und hatte somit ein hohes Risiko für unerwünschte Wirkungen. Die Verteilung spezifischer Begleiterkrankungen war innerhalb der Behandlungsgruppen ähnlich (Tab. 2 und Abb. 1).
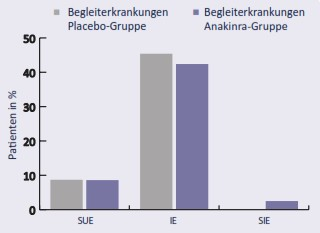
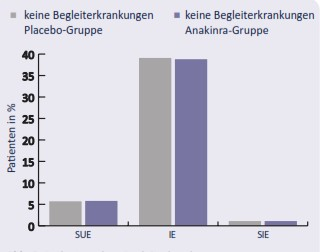
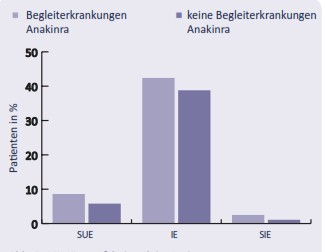
Die Abbildungen 2–4 zeigen die Inzidenzraten von SUE, IE und SIE in der Gruppe der Patienten mit Begleiterkrankungen, die entweder Anakinra oder Placebo erhielten (Abb. 2), in der Patientengruppe ohne Begleiterkrankungen, die ebenfalls Anakinra oder Placebo erhielten (Abb. 3), und zu Vergleichszwecken in den beiden Patientengruppen mit oder ohne Begleiterkrankungen, die Anakinra erhielten (Abb. 4).
Niedrige Rate infektiöser Ereignisse
Die Inzidenz von Infektionen (IE) bei Hochrisiko-Patienten, verglichen mit Patienten ohne Begleiterkrankungen, war sowohl in der mit Placebo als auch in der mit Anakinra behandelten Gruppe ähnlich erhöht. Die Inzidenz von IEs in der Placebo-Gruppe schien leicht höher zu sein im Vergleich zur Anakinra-Gruppe.
Bei Hochrisiko-Patienten, die Anakinra erhielten, zeigte sich eine leicht erhöhte Anzahl von schweren infektiösen Ereignissen (SIE, Abb. 2) im Vergleich zu Patienten, die Placebo erhielten. Ungewöhnliche oder opportunistische Infektionen wie Tuberkulose, Histoplasmose, Listeriose und Aspergillose wurden in dieser Studie nicht beobachtet. Mit 2,5 % ist die Inzidenz-Rate für SIE in dieser Studie vergleichbar mit der zuvor berichteten Rate unter Anakinra-Therapie in der gesamten Patientenpopulation, unabhängig von Begleiterkrankungen (2,1 % im Vergleich zu 0,4 % bei Placebo).
Fazit
In dieser Studie zu Hochrisiko-Patienten traten SUE bei Patienten, die Placebo erhielten, genauso oft ein (8,7%) wie bei Patienten, die Anakinra erhielten (8,6%). Die Inzidenz spezifischer SUEs war gering. Patienten mit aktiver RA und Begleiterkrankungen haben unter der Behandlung mit Anakinra offensichtlich kein erhöhtes Risiko für ein schwerwiegendes Ereignis verglichen mit Patienten ohne Begleiterkrankungen, was die Schlussfolgerung nahe legt, dass die Behandlung mit Anakinra bei diesen Hochrisikopatienten gut vertragen wird.
Vergleich der unerwünschte Wirkungen mit anderen Biologika
In einer 2011 von Singh und Kollegen durchgeführten Analyse Adverse effects of biologics: a network meta-analysis and „Cochrane overview wurden unerwünschte Wirkungen von TNF-Blockern (Etanercept, Adalimumab, Infliximab, Golimumab, Certolizumab), dem Interleukin (IL)-1 Antagonisten (Anakinra), dem IL-6 Antagonist (Tocilizumab), dem anti-CD28 (Abatacept), und der gegen B-Zellen gerichteten Therapie (Rituximab) bei Patienten mit allen Erkrankungen außer HIV/AIDS miteinander verglichen. Dabei kommen die Autoren zur der Schlussfolgerung, dass in diesem indirekten Vergleich Abatacept und Anakinra mit einem signifikant niedrigeren Risiko für schwere unerwünschte Wirkungen verbunden waren als die meisten anderen in diese Untersuchung einbezogenen Biologika.
Weitere Studien
In weiteren Studien, u.a. auch aus der klinischen Praxis (Langer und Missler-Karger 2003, den Broeder et al 2006), Extensionsstudien (Fleischmann et al 2006) sowie Metaanalysen (Mertens et al 2009) ergaben sich keine neuen Sicherheitssignale, die über die aus den vorherigen Studien bekannten unerwünschten Wirkungen (Nebenwirkungen) hinausgingen.
Unsere Seiten zu Anakinra (Kineret)
Kurzbeschreibung
Anwendungsgebiete
Praktische Durchführung
Impfungen, Schwangerschaft und Stillzeit
Praktische Tipps
Literatur zur Sicherheit von Anakinra bei der RA
- Cohen S, Hurd E, Cush J, et al. Treatment of rheumatoid arthritis with anakinra, a recombinant human interleukin-1 receptor antagonist, in combination with methotrexate: results of a twenty-four-week, multicenter, randomized, double-blind, placebo-controlled trial. Arthritis Rheum 2002; 46: 614-24 Link
- den Broeder AA, de Jong E, Franssen MJ, Jeurissen ME, Flendrie M, van den Hoogen FH. Observational study on efficacy, safety, and drug survival of anakinra in rheumatoid arthritis patients in clinical practice. Ann Rheum Dis. 2006 Jun;65(6):760-2 Link
- Fleishmann RM. Safety of anakinra, a recombinant interleukin-1 receptor antagonist (r-metHuIL-1ra), in patients with rheumatoid arthritis and comparison to anti-TNF-alpha agents. Clin Exp Rheumatol. 2002 Sep-Oct;20(5 Suppl 27):S35-41. Link
- Fleischmann RM, Schechtman J, Bennett R, et al. Anakinra, a recombinant human interleukin-1 receptor antagonist (r-metHuIL-1ra), in patients with rheumatoid arthritis: a large, international, multicenter, placebo-controlled trial. Arthritis Rheum. 2003; 48, 927–94 Link
- Rubbert-Roth A. Addressing the safety of anakinra in patients with rheumatoid arthritis. Rheumatology (Oxford). 2003 May;42 Suppl 2:ii29-35. Link
- Fleischmann RM, Tesser J, Schiff MH, Schechtman J, Burmester GR, Bennett R, Modafferi D, Zhou L, Bell D, Appleton B. Safety of extended treatment with anakinra in patients with rheumatoid arthritis. Ann Rheum Dis. 2006 Aug;65(8):1006-12 Link
- Genovese M C, Cohen S B, Moreland L, Lium D, Robbins S, Newmark R. et al Combination therapy with etanercept and anakinra in the treatment of patients with rheumatoid arthritis who have been treated unsuccessfully with methotrexate. Arthritis Rheum. 2004 May;50(5):1412-9 Link
- Jiang Y, Genant HK, Watt I, et al. A multicenter, double-blind, dose-ranging, randomized, placebo-controlled study of recombinant human interleukin-1 receptor antagonist in patients with rheumatoid arthritis: radiologic progression and correlation of Genant and Larsen scores. Arthritis Rheum 2000; 41: 2196-204 Link
- Langer HE, Missler-Karger B. Kineret: efficacy and safety in daily clinical practice: an interim analysis of the Kineret response assessment initiative (kreative) protocol. Int J Clin Pharmacol Res. 2003;23(4):119-28. Link
- Mertens M, Singh JA. Anakinra for rheumatoid arthritis. Cochrane Database Syst Rev. 2009 Jan 21;(1):CD005121. Link
- Schiff MH, DiVittorio G, Tesser J, et al. The safety of anakinra n high-risk patients with active rheumatoid arthritis. six-month observations of patients with comorbid conditions. Arthritis Rheum 2004; 50: 1752-60 Link
- Singh JA, Wells GA, Christensen R, Tanjong Ghogomu E, Maxwell L, MacDonald JK, Filippini G, Skoetz N, Francis D, Lopes LC, Guyatt GH, Schmitt J, La Mantia L, Weberschock T, Roos JF, Siebert H, Hershan S, Lunn MPT, Tugwell P, Buchbinder R. Adverse effects of biologics: a network meta-analysis and Cochrane overview (Review) Cochrane Database Syst Rev. 2011 Feb 16;(2):CD008794 Link
- Tesser J, Fleischmann R, Dore R, Bennett R, Solinger A, Joh T, Modafferi D, Schechtman J; 990757 Study Group. Concomitant medication use in a large, international, multicenter, placebo controlled trial of anakinra, a recombinant interleukin 1 receptor antagonist, in patients with rheumatoid arthritis. J Rheumatol. 2004 Apr;31(4):649-54. Link
- Thaler K, Chandiramani DV, Hansen RA, Gartlehner G. Efficacy and safety of anakinra for the treatment of rheumatoid arthritis: an update of the Oregon Drug Effectiveness Review Project. Biologics. 2009;3:485-98. Epub 2009 Dec 29. Link